O celulă hiperactivă din creier ar putea declanșa boala Alzheimer
#Postat de Antoniu Lovin on februarie 1, 2022
Totul a început cu date genetice. O genă aici, o genă acolo. În cele din urmă, povestea a devenit mai clară: dacă oamenii de știință vor găsi într-o zi un remediu pentru boala Alzheimer, ar trebui să se uite la sistemul imunitar. În ultimele două decenii, cercetătorii au identificat numeroase gene implicate în diferite funcții ale sistemului imunitar care pot contribui, de asemenea, la apariția bolii Alzheimer. Unii dintre principalii suspecți sunt genele care controlează mici celule imunitare umile numite microglia, acum în centrul cercetării intense în dezvoltarea de noi medicamente pentru Alzheimer. Microglia sunt celule asemănătoare amibei care scrutează creierul pentru leziuni și invadatori. Ele ajută la curățarea celulelor cerebrale moarte sau afectate și ”înghit” literalmente microbii invadatori. Fără ei, am avea probleme. Într-un creier normal, o proteină numită beta-amiloid este îndepărtată prin sistemul nostru limfatic de către microglia ca gunoi moleculare. Dar uneori se acumulează.
Anumite mutații ale genelor sunt unul dintre vinovații acestei acumulări toxice. Leziunile traumatice ale creierului sunt o altă funcție microglială și, probabil, afectarea funcției microgliale. Un lucru asupra căruia toată lumea este de acord este că, la persoanele cu Alzheimer, prea mult amiloid se acumulează între celulele creierului și în vasele care alimentează creierul cu sânge. Odată ce amiloidul începe să blocheze rețelele de neuroni, declanșează acumularea unei alte proteine, numită tau, în interiorul acestor celule cerebrale. Prezența tau trimite microglia și alte mecanisme imunitare în exces, ducând la răspunsul imunitar inflamator despre care mulți experți cred că în cele din urmă scade vitalitatea creierului în boala Alzheimer. Până în prezent, aproape o duzină de gene implicate în funcția imunitară și microglială au fost legate de boala Alzheimer. Primul a fost CD33, identificat în 2008. „Când am primit rezultatele am fugit la biroul colegului meu de alături și am spus că trebuie să vezi asta!” spune neurologul de la Harvard Rudolph Tanzi. Tanzi, a condus cercetarea CD33. Descoperirea a fost numită rapid o descoperire medicală de top din 2008 de revista Time. „Am râs pentru că ceea ce ei nu știau este că nu aveam idee ce face această genă”, glumește el. Dar, de-a lungul timpului, cercetările efectuate de Tanzi și grupul său au dezvăluit că CD33 este un fel de comutator microglial pornit-oprit, activând celulele ca parte a unei căi inflamatorii. „Am pus totul în funcțiune când a venit vorba de genetică”, spune el. Microglia recunoaște în mod normal modelele moleculare asociate cu microbii și daunele celulare ca fiind nedorite. Acesta este modul în care știu ei să ia măsuri – să devoreze agenți patogeni necunoscuti și țesuturi moarte. Tanzi crede că microglia simte orice semn de afectare a creierului ca o infecție, ceea ce le face să devină hiperactive. O mare parte din sistemul nostru imunitar uman modern, explică el, a evoluat cu multe sute de mii de ani în urmă. Durata noastră de viață la acea vreme era mult mai scurtă decât este în prezent și majoritatea oamenilor nu trăiau suficient de mult pentru a dezvolta demență sau celulele creierului ofilite care sunt asociate cu aceasta. Deci, sistemul nostru imunitar, spune el, presupune că orice țesut cerebral defect se datorează unui microbi, nu demenței. Microglia reacționează agresiv, curățând zona pentru a preveni răspândirea infecției. „Ei spun: „Mai bine ștergem această parte a creierului care este infectată, chiar dacă nu este. Ei nu știu”, glumește Tanzi. „Aceasta este ceea ce cauzează neuroinflamația. Și CD33 activează acest răspuns. Microglia devin ucigași, nu doar îngrijitori”.
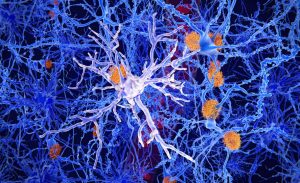
Dacă CD33 este yin, o genă numită TREM2 este yang. Descoperit la câțiva ani după CD33, TREM2 controlează activarea microglială, readucendu-le la rolul lor de menajere celulare. Neurologul David Holtzman de la Universitatea Washington din St. Louis, care studiază TREM2, este de acord că acolo unde găsești celule amiloide, tau sau moarte ale creierului, există microglia, nerăbdătoare de plecare și gata să curețe. „Cred că la început mulți oameni au crezut că aceste celule reacționează la patologia Alzheimer și nu neapărat o cauză a bolii”, spune el. Descoperirea TREM2 pe călcâiele CD33 a fost cea care a schimbat cu adevărat gândirea, în parte pentru că produce o proteină care în creier se găsește doar în microglia. Genele sunt întinderi de ADN care codifică proteinele care ne conduc literalmente corpurile și creierul. „Mulți dintre noi [în domeniu] au spus imediat „Uite, acum există un factor de risc care este exprimat doar în microglia. Așa că trebuie să fie că celulele imune înnăscute sunt importante într-un anumit fel în patogeneza bolii”, adaugă el. Holtzman vede activarea microglială în demența iminentă ca pe o sabie cu două tăișuri. La început, microglia elimină amiloidul nedorit pentru a menține sănătatea creierului. Dar odată ce amiloidul și tau-ul acumulate au făcut destule daune, neuroinflamația care vine cu activarea microglială face mai mult rău decât bine. Neuronii mor în masă și demența se instalează.
Nu toți cercetătorii sunt convinși. Serge Revist este profesor la Departamentul de Medicină Moleculară de la Facultatea de Medicină a Universității Laval din Quebec. Pe baza cercetărilor din laboratorul său, el crede că, deși activitatea imunitară afectată este implicată în Alzheimer, aceasta nu este cauza principală. „Nu cred că celulele imune provoacă daune, încă mai cred că beta-amiloidul în sine”, spune el, „În laboratorul meu, în studiile la șoareci, nu am descoperit niciodată că celulele imune sunt direct responsabile pentru uciderea neuronilor”. El crede că, la unii pacienți cu Alzheimer, microglia nu poate face față excesului de amiloid care se acumulează în boală și că dezvoltarea de tratamente care îmbunătățește capacitatea microgliei și a sistemului imunitar de a elimina proteina ar putea fi eficientă.
 Jurnal FM
Jurnal FM 





